即使是小学的自然课,也会讲到固液气三态和相变,最显然的例子是水:冰,液态水,水蒸汽,在一个大气压下,水零度结冰,100度沸腾,这也是摄氏温标(Celsius, or centigrade scale) 的定义。固体到液体是熔化(fusion),液体到气体是气化(vaporization), 这两个用水都能很好演示,那么固体到气体是升华,这个就不好演示了。二氧化碳干冰这玩意容易冻伤人不安全,所以他们就会用碘演示升华。碘又是有颜色的东西,升华出紫气,非常有王八之气。
既然碘是升华,直接固体到气体,那是不是碘在常压下没有液体状态呢?就像二氧化碳那样?
https://haygot.s3.amazonaws.com/questions/2015801_1913491_ans_df4daf9c6e9546e58fe9afa9be54e613.JPG
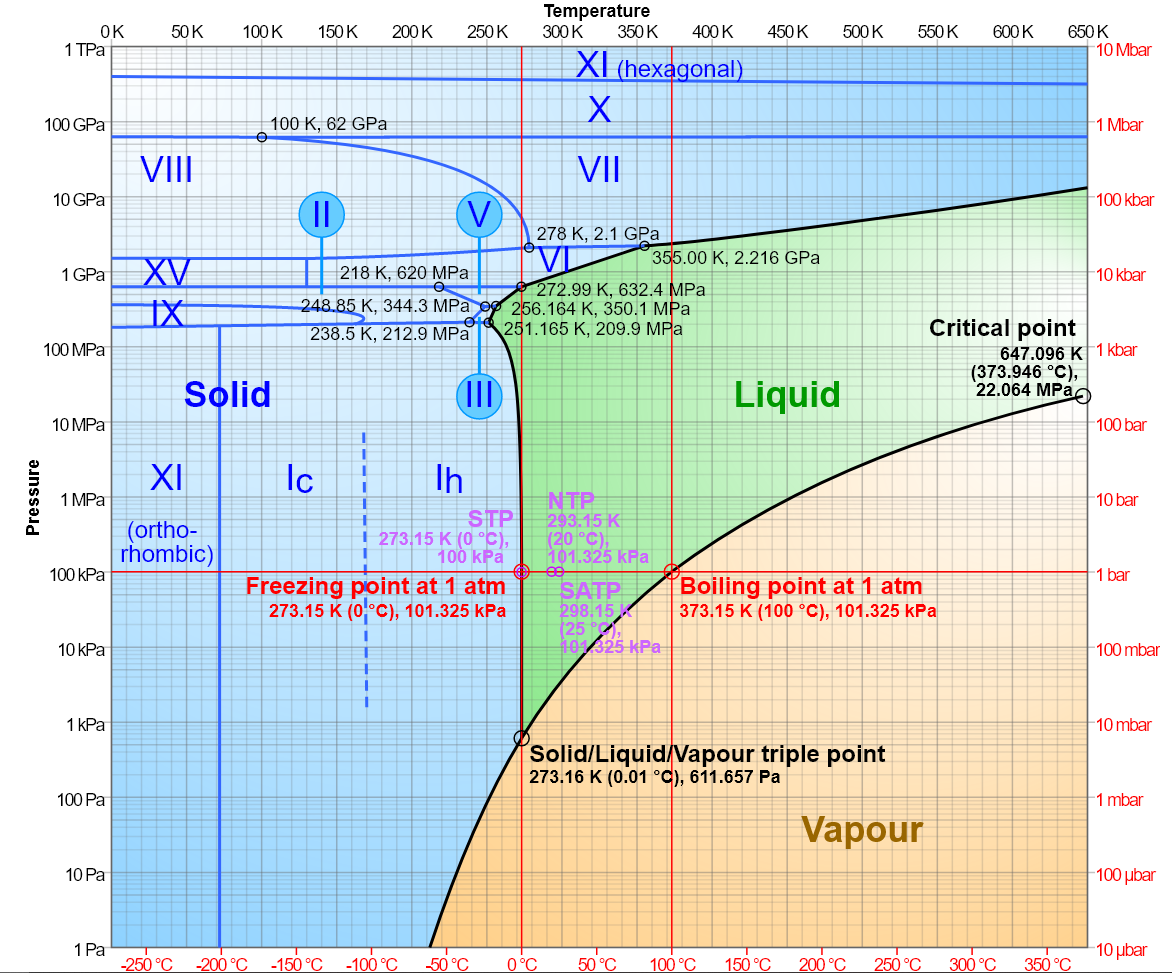
如图,左为水的相图,在一个大气压下常压加热冰,冰先化水,然后水再煮沸为水蒸汽。
右为二氧化碳的相图,在一个大气压下常压加热干冰,干冰直接变成二氧化碳气体,升华温度为零下78摄氏度。要得到液态二氧化碳,必须加压到5.1个大气压以上,才有液态二氧化碳。因为二氧化碳三相点(固液气三相共存点,triple point)气压大于一个大气压,所以常压下二氧化碳不存在液态。
所以一般人就会误解,觉得碘的相图也是二氧化碳这样的,常压下加热碘,碘就会直接从固体变成气体,不会有液体阶段。
https://uwaterloo.ca/chem13-news-magazine/sites/ca.chem13-news-magazine/files/uploads/images/october-2015-article-3-graph-sublimation_page_04.jpg
但是这才是碘的相图,和水相图类似,三相点都在一个大气压以下,所以加热碘,会进入液态,然后气态。
所以,是大家的记忆错了吗?
youtu.be/dPIaEWd8zf4实验室现场加热,碘果然先熔化再气化。
那课本上说的”碘升华“错了吗?
没有,如果我们把三种相变叫做熔化,气化,升华,那碘在常压下确实可以不经液态直接变气体;这是因为气化和升华都有两种方式,热力学平衡的,和热力学非平衡的。液体气化的两种方式,我们称为沸腾(boiling)和蒸发(evaporation),前者如烧开水,后者如涂清凉油到皮肤上蒸发冷却。前者是热力学平衡的,就是把液体加热到沸点,这时候液体变气体,气体变液体没有任何热力学的壁垒,可以任意转化。后者是热力学非平衡的,比如在地面上一摊水,不断有水分子逸出到空气里,随着空气流动被带走,而这些水蒸汽没法在液面上空累积,所以没法阻止水进一步蒸发,最后就是地面上这摊水全干了,而气温离沸点差得远呢。那么对于固体的升华,我们并没有区分碘固体常温下变气体,和二氧化碳在一个大气压下,零下78度变气体这两种情况。前者类似地上的水蒸发,后者对应烧开水烧到100度。所以名词的混用导致了印象的错位。因为升华一词不区分热力学平衡下的固体变气体(干冰),和热力学非平衡下的固体变气体(碘),因此观察到后者的人,误以为实际上的行为类似前者。
冰在常温常压下,蒸气压很低,所以观测不到显著的冰升华现象,而碘则有显著的蒸气压,所以可以观测到碘的升华,而常温下干冰的蒸气压高得一塌糊涂,所以放在室温下干冰迅速升华,留下一大片被冷却的水蒸汽变成的雾。
其实要更好的理解物质的相和相变,要从热力学上来理解。物质形成均匀的一坨,叫做一个相(phase),相变就是物质从一相变成另一相,变化的条件就是“能量”越低越好,这里的能量,是指自由能,即“可以用来做功的能量”,在定体积条件下,是Helmholtz Free Energy, A=U-TS, 在定压强条件下(也是化学中最常用的条件),是Gibbs Free Energy, G=H-TS=A+PV.
一看就知道自由能受两个因素影响,第一个是和温度(基本)无关项,就是内能,内部作用越强,能量就越低(绑得紧),比如固体就最低,气体就最高(接近零);第二个和温度有关,就是熵,无序程度越高,熵就越高,比如固体熵就低,气体熵就高。那么这两个项相互竞争,就和温度有关,温度越低,熵部分越不重要,所以物质偏向于能量低的状态,比如说固态;而温度越高,熵部分就越重要,所以物质偏向无序度高的状态,也就是气态。不同相的自由能相等,就是两相达到均衡,这时候物质就处于两相共存的状态,比如冰水混合物在0度,水和蒸汽混合物在100度一个大气压。
那为什么液体可以挥发,而固体中像碘一样升华的不多呢?因为对于温度低于沸点的液体,它仍然有机制让液体分子变成气体。固然,在这个状态下,物质更容易处于自由能较低的液态,而不是自由能较高的气态。但是由于组成物质的微观成分(分子)在不停的无规律运动,总有分子逃出液体表面变成气体,也总有气体分子撞击液体表面被液体俘获。这个过程也会达到平衡,比如水在25度的时候,它达到这个平衡时水蒸汽压强是23.8torr(也就是说当环境气压下降到这个压强的时候,25度的水就会沸腾)。因此如果维持水在25度的话,水和蒸汽达成平衡,水不会自发的全部变成气体。但是为什么地上的水会消失呢?因为周围环境是变动的,水蒸汽被交换的气体带走,导致水面上水的蒸气压低于平衡的蒸气压,于是为了平衡,更多的水蒸发为气体,周而复始,直到所有液态水全部蒸发完毕。这个就是化学的Le Chatelier原理,类似于电磁学的楞次定律(Lenz's Law)。都是一个套路,就是系统受到扰动之后,就改变平衡状态试图抵消这种扰动。
固体的蒸气压一般很低,因为固体不像液体一样分子间作用力弱,而液体表面上分子作用力更弱。固体的晶格结构让固体表面的分子仍然受到较强的作用力,因此很难蒸发,但是碘的颜色太鲜明了,即使其常温下蒸气压只有0.20torr, 但是由于鲜艳的紫色,我们可以看到这个升华的碘蒸汽,而常温下碘是固体,因此我们看到了碘的升华。